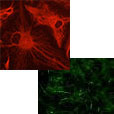
iPS細胞由来神経系細胞を用いて、筋萎縮性側索硬化症 (ALS) やアルツハイマー病 (AD) を始めとする神経系の疾患モデルの構築と薬剤評価系を提供します。また、細胞老化技術や神経細胞/アストロサイト/ミクログリア共培養技術を活用し、お客様のご要望に応じた薬効評価系構築が可能です。
【委託実績】
エーザイ株式会社をはじめとする大手製薬メーカーから多数の委託実績を有しております。
また、ベンチャー企業やアカデミアからも幅広くお問い合わせをいただいており、信頼と実績のあるサービスを提供しております。
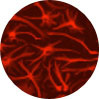
ALSモデル (運動神経細胞 × 酸化ストレス)
ALSモデルとなり得る酸化ストレスによる神経傷害の系を用いて、化合物評価が可能です。
独自の酸化
ストレス誘導法-
酸化ストレスなし 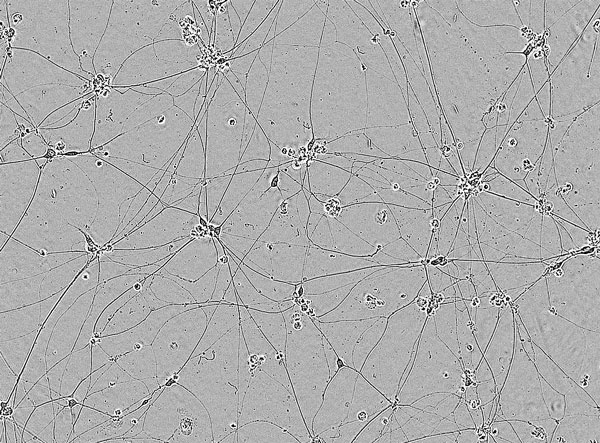
酸化ストレスあり 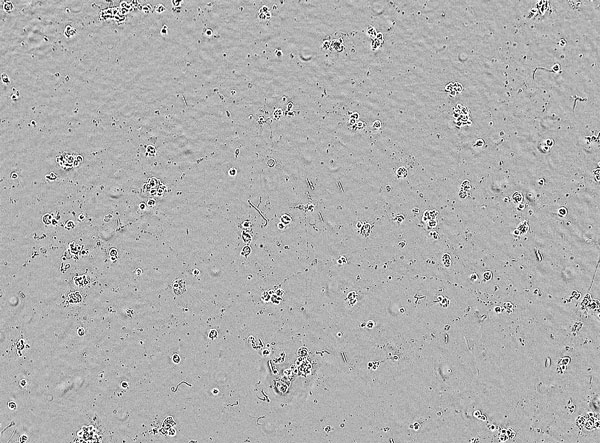
ストレス+エダラボン 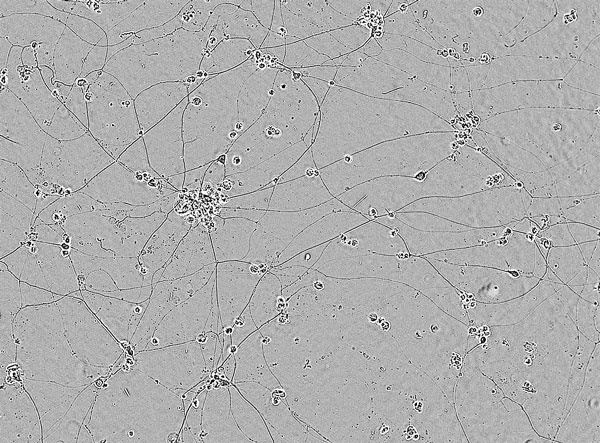
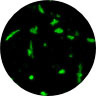
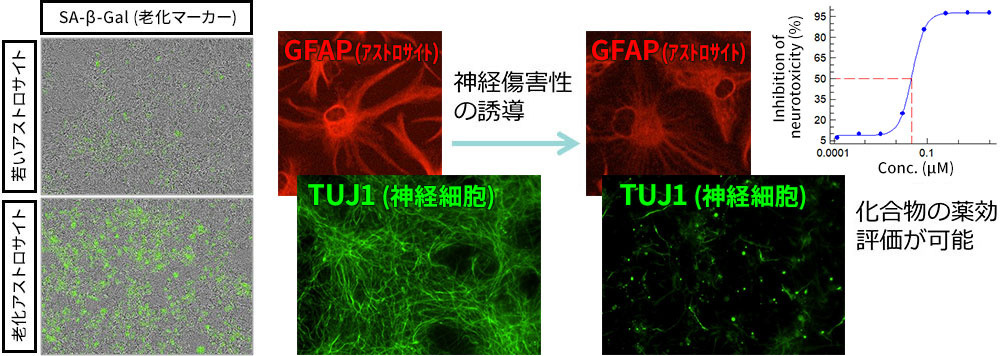
神経変性疾患モデル (神経傷害性老化アストロサイト × 神経細胞)
神経変性疾患モデルとなり得る神経傷害性アストロサイトによる神経細胞死誘導の系を用いて、化合物評価や探索、ネットワーク解析による疾患理解・新規標的探索、標的確認が可能です。
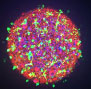
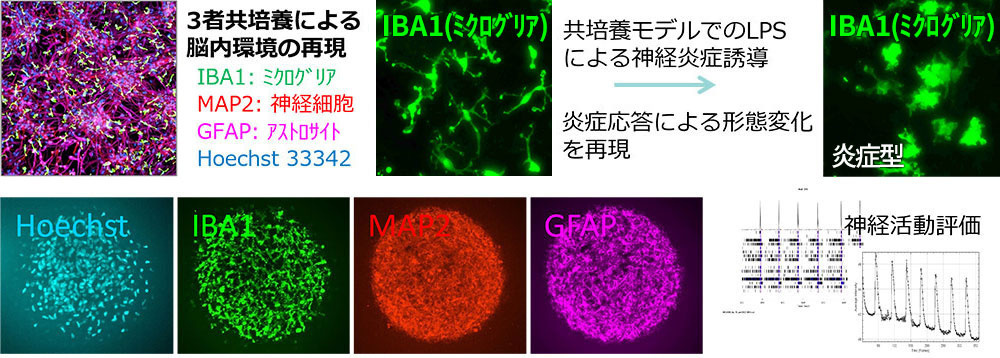
共培養モデル・神経炎症モデル (ミクログリア × アストロサイト × 神経細胞)
ミクログリア x アストロサイト x 神経細胞の3者共培養により、脳内環境を再現し、神経炎症カスケードの可視化や、Ca2+イメージングにて神経活動評価が可能です。
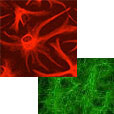
新規試験系の構築
お客様のご要望に合わせた試験系のご提案が可能です。
まずはご相談ください。
- Human-iPSC derived Neural Cells
-
 Glutamatergic
Glutamatergic
Neurons Dopaminergic
Dopaminergic
Neurons Motor Neurons
Motor Neurons
-
-
 Co-/Tri-culture
Co-/Tri-culturemodel establishment

- Mono-culture
-
Neuron

Neurite length analysis 
Oxidative stress-induced damage model 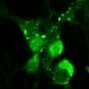
TDP-43
aggregation
Aβ/tau/p-tau ELISA -
Astrocyte
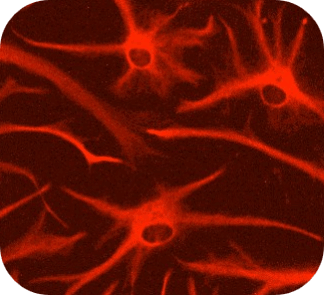

Senescent astrocyte model 
Neurotoxic astrocyte model 
Gene KD -
Microglia
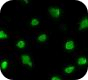
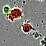
Aβ phagocytosis assay 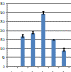
Cytokine ELISA
- Co-culture
-
Neuron/Astrocyte
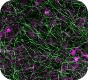
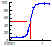
Astrocyte neurotoxicity assay 
Ca2+ imaging 
MEA -
Microglia/Astrocyte
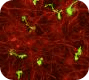

Morphology assay 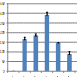
Cytokine ELISA
- Tri-culture
-
Neuron/Astrocyte/Microglia

Neuroinflammation assay 
Ca2+ imaging


Diseases areas
- Alzheimer’s disease
- Parkinson’s disease
- Amyotrophic Lateral Sclerosis (ALS)
- Neuroinflammation
- Neurodegeneration
- Pain
Research models
- Human iPSC-derived Neuron cells (GABA, Gluta, Dopa, Motor)
- Human iPSC-derived Microglia
- Human iPSC-derived Astrocytes
- Additional iPSC models and custom
- 2D & 3D models in Mono-, Co- and Tri-culture
- Neuroinflammation in tri-culture models
- Oxidative stress-induced neuronal damage model
- Neurotoxic astrocyte model
- Custom models based on your needs
- BBB models
Readout / Analysis
- High-content imaging analysis
- High Throughput Screening
- qRT-PCR & Digital PCR
- ECL-ELISA (MSD assays)
- Electrophysiology (MEA)
- Calcium Imaging
- Cytokine release/profiling
- RNAi screening
- Gene regulation
- Transcriptome analysis
- Gene Network analysis and MOA
- Cell morphology and cellular localization analysis
- EV extraction
- Autophagy/mitophagy assay
- Aβ phagocytosis assay
- Neurite outgrowth assay
- Astrocyte neurotoxicity assay
- TDP-43 aggregation and more
関連製品
iPS 細胞のリーディングカンパニーであるFUJIFILM Cellular Dynamics, Inc. にて、各種ニーズに応える iCell® 製品 (iPS 細胞由来分化細胞) をラインアップしております。
関連ページ
富士フイルムの神経研究に関する歴史
富士フイルムグループの中枢神経系疾患創薬への取り組み
当社は、2000年代初頭、写真フィルム市場の縮小を見据え、新たなビジネス機会を模索し始めました。その一環として、2008年に、感染症および中枢神経系疾患を主要な疾患領域として創薬活動に取り組む富士フイルム富山化学をグループに加え、創薬分野への参入を果たしました。
患者由来ヒトiPS細胞を活用した創薬プラットフォーム構築:グループ会社間シナジー
当社は、富士フイルム富山化学との連携を強化するとともに、アカデミアなど外部専門機関とも協力し、患者由来のヒトiPSC由来神経細胞を用いた薬剤評価システムの構築に取り組んできました。この取り組みにより、ヒトiPS細胞を次世代創薬プラットフォームとして活用するための強固な基盤を築くことができました。さらに、2015年にヒトiPSC由来分化細胞を開発・製造する米国FUJIFLM Cellular Dynamics, Inc.をグループ会社として迎えました。世界中の研究者との協働により、ヒトiPS細胞を用いた創薬プラットフォームを深化させています。
薬理研究者と計算生物学研究者の協働による革新的な遺伝子ネットワーク解析
当社は、独自のアルゴリズム、高度な変数圧縮技術、高性能スーパーコンピューティングリソース、また薬理研究者および計算生物学研究者の協働により、複雑な生物学的相互作用を解読するための革新的な遺伝子ネットワーク解析技術を確立しました。本技術は、薬剤作用機序仮説の設定や、重要な遺伝子ターゲットの特定を実現し、創薬研究の加速に貢献します。
自社創薬から創薬支援CROビジネスへの転換
2020年以降、当社は当社グループ企業との連携を通じて、創薬から医薬品製造までを支援する事業に転換しました。この転換により、特に中枢神経系疾患の長年にわたる創薬経験と技術プラットフォームを活用した創薬支援サービスを開始しました。
私たちは、Partners for Lifeを掲げ、お客様の革新的な創薬加速に貢献いたします。
ポスター
| 年度 | 学会名 | 演題 | 概要 | |
|---|---|---|---|---|
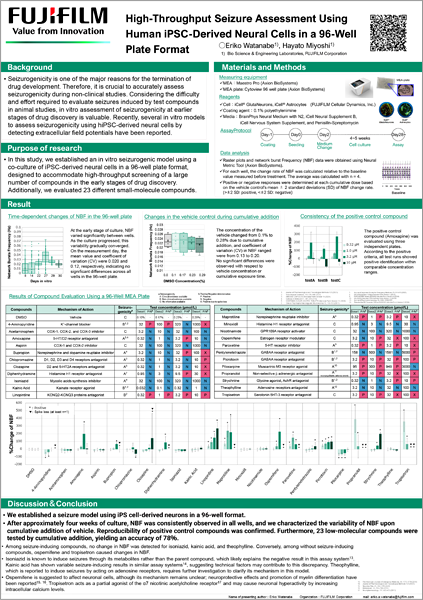 |
2026 | 第17回日本安全性薬理研究会学術年会 | High-Throughput Seizure Assessment Using Human iPSC-Derived Neural Cells in a 96-Well Plate Format | |
 |
2025 | 第16回安全性薬理学会 | Development of a Seizure Assessment Model Using Human iPSC-Derived Neural Cells. | Axion BioSystems 社の Maestro Pro を用いた iCell グルタミン酸作動性神経細胞と iCell アストロサイト共培養モデルの痙攣誘発性化合物に対する電気生理応答評価です。痙攣誘発性化合物を臨床的な濃度範囲で単回もしくは漸増処置した際の細胞集団のネットワークバースト変化を評価しています。 iCell グルタミン酸作動性神経細胞と iCell アストロサイト を用いた本評価法は、臨床で報告があった神経毒性と高い相関性を有するin vitro 神経毒性評価手法として活用可能です。 |
| 2025 | 第48回日本神経科学大会 | Parkinson’s disease (PD) model using the iPSC-derived tri-culture system of neurons, astrocytes, and microglia stimulated with alpha-synuclein oligomer (H. Kobayashi, M. Taniguchi, S. Endoh-Yamagami) | パーキンソン病は中脳黒質のドーパミン神経の変性と、α-シヌクレインの凝集と蓄積を特徴とする疾患である。本研究では、iPS細胞由来神経細胞、アストロサイト、ミクログリアの三者共培養系を構築し、α-シヌクレインオリゴマーを添加することにより、ミクログリアの活性化を伴う神経炎症が誘導されることを示した。本病態モデルは、パーキンソン病の分子メカニズムの理解や新たな治療薬開発に有用なものである。 | |
| 2025 | 第48回日本神経科学大会 | TDP-43 aggregation induction by protein homeostasis disturbance in iPSC-derived neurons (H. Kobayashi, H. Munezane, S. Endoh-Yamagami) | iPS細胞由来神経細胞を用いて、タンパク質恒常性を乱す化合物が、TDP-43タンパク質の凝集を誘導することを見出し、処置時間依存的にTDP-43凝集が増加することを定量的に示した。また、TDP-43凝集体誘導時にSTMN2 mRNA量が減少し、cryptic STMN2エクソンが増加することを確認した。さらに、既知化合物が凝集体形成を抑制することを確認した。このTDP-43凝集誘導系はALS治療薬開発に有用であると期待できる。 | |
| 2025 | IDDST 2025 | Glia-Oriented Approaches to Drug Development for Neurodegenerative Diseases (S. Endoh-Yamagami) | アストロサイトは本来神経細胞を保護する細胞であるが、神経傷害性アストロサイトの神経変性疾患への関与が注目されている。ヒトiPSC由来アストロサイトを用いて、げっ歯類での条件とは異なるサイトカイン類の組合せにより、強い神経傷害性を誘導した。市販化合物のスクリーニング、siRNAノックダウンによるヒット化合物の標的バリデーションを行った。さらに、神経傷害性誘導時の遺伝子発現ネットワーク解析を行い、その結果から、新たな標的候補分子を見出した。神経変性疾患の新規治療薬開発への有用性が期待できる。 | |
| 2024 | Society of Neuroscience | Ferroptosis-dependent neuronal damage induced by oxidative stress and TDP-43 aggregation formation in iPSC-motor neurons as ALS models (Hayato Kobayashi, Hitoshi Suzuki-Masuyama, Hirokazu Tanabe, Hiroshi Kato, and Setsu Endoh-Yamagami) | 筋萎縮性側索硬化症(ALS)を含む神経変性疾患の細胞評価系が求められている。ヒトiPS細胞由来の運動神経細胞を弱い酸化ストレス存在下で培養することにより、神経細胞傷害の誘導に成功し、ALS既存薬エダラボンが薬効を示すことを確認した。神経細胞死の様式を阻害剤を用いて解析したところ、フェロトーシス阻害剤が神経保護効果を示すことを見出した。さらに、化合物刺激を用いて、ALS病態として注目されているTDP-43の凝集を再現した結果についても報告した。 | |
| 2024 | Society of Neuroscience | iPSC-derived senescent astrocytes generate inflammation prone environment and they are more sensitive to cytokines inducing a neurotoxic state (H. Kobayashi, T. Wakui, H. Kato, S. Endoh-Yamagami) | 加齢は神経変性疾患の最大のリスクファクターであり、加齢の特徴である老化に関する研究は神経変性疾患の理解に非常に重要である。iPS細胞の発明により脳の細胞を比較的容易に入手できるようになったが、iPS細胞はリプログラミングの過程で老化がリセットされてしまう課題があった。本研究ではiPS細胞由来の老化アストロサイトを作製し、神経炎症との関りや、神経変性疾患に深く関与する神経傷害性アストロサイトとの関係を評価した。本研究成果は加齢性の神経変性疾患の病態理解に有用なものである。 | |
| 2024 | NEURO2024 (第47回日本神経科学大会) | Ferroptosis-dependent neuronal injury induced by oxidative stress in iPSC-derived motor neurons as ALS model (H. Kobayashi, H. Suzuki-Masuyama, H. Tanabe, H. Kato, S. Endoh-Yamagami) | ヒトiPS細胞由来の運動神経細胞を弱い酸化ストレス存在下で培養することにより、神経細胞傷害の誘導に成功した。また、ALS既存薬エダラボンやフェロトーシス阻害剤が神経保護効果を示すことを確認した。さらに、化合物スクリーニングによりコレステロール合成阻害剤が薬効を示すこと、コレステロール合成に関わる酵素を欠失させた神経細胞では薬効が消失することを示した。確立した細胞評価系は、ALS治療薬開発や病態理解に有用であると期待する。 | |
| 2024 | NEURO2024 (第47回日本神経科学大会) | Study of glial function on neuronal activity under neuroinflammation in neuron/astrocyte/microglia tri-culture system (H. Kobayashi, H. Kato, S. Endoh-Yamagami) | 神経炎症は様々な神経変性疾患に関与し、ミクログリアやアストロサイトのようなグリア細胞が中心的な役割を果たすことが知られている。本研究ではiPS細胞由来の神経細胞、アストロサイト、ミクログリアを用いた三者共培養系を用いて神経炎症を再現し、神経活動に対する神経炎症やグリア細胞の影響を評価した。本研究成果は神経炎症関連疾患の病態理解に有用なものである。 | |
| 2024 | NEURO2024 (第47回日本神経科学大会) | Evaluation system for seizure risks using a co-culture system consisting of human iPS cell-derived neurons and astrocytes (M. Taniguchi, H. Kobayashi, S. Endoh-Yamagami) | 痙攣は非臨床段階での発生頻度が最も多い神経毒性であるが、痙攣リスクの評価は動物試験に依存しており、種差やスループットの観点よりヒトin vitro評価系が求められている。ヒトiPS細胞由来の神経細胞、アストロサイトからなる共培養システムを用いて、カルシウムイメージングを行い、既知の痙攣リスク化合物を評価した結果を報告する。 | |
| 2023 | Society of Neuroscience | Neurotoxic human iPSC-astrocytes and gene expression network analysis to identify drug targets for neurodegenerative diseases (Hayato Kobayashi, Kiyohiro Maeda, Kenichi Kazetani, Akira Nabetani, Setsu Endoh-Yamagami) | 様々な年齢のヒト脳の遺伝子発現データを用いて、遺伝子発現ネットワーク解析を行い、加齢に伴いミクログリアの活性化、それに続くアストロサイトの活性化が起こることを示した。さらに、ヒトiPS細胞由来アストロサイトを用いて神経傷害性アストロサイトを誘導し、その誘導時の遺伝子ネットワーク解析により神経変性疾患に対する新たな薬剤標的候補を見出し、siRNAにより標的を絞り込んだ結果について報告する。 | |
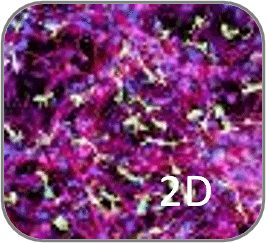
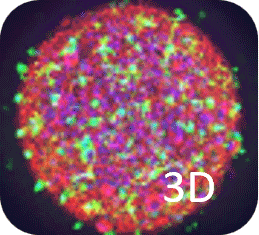
| 2023 | Society of Neuroscience | 2D and 3D tri-culture systems for investigation of cellular interaction among neurons, astrocytes, and microglia (Hayato Kobayashi, H. Kato, Setsu Endoh-Yamagami) | 脳は神経細胞とグリア細胞 (アストロサイト、ミクログリア、オリゴデンドロサイト) から構成され、脳機能や病態形成にはこれらの細胞の相互作用が重要である。本研究ではiPS細胞由来神経細胞、アストロサイト、ミクログリアの三者共培養系を構築し、神経炎症誘導によるミクログリアの形態変化や、ミクログリアとアストロサイトの細胞間相互作用を確認した。本培養系は、中枢神経系の細胞間相互作用の評価を可能とし、脳の本来の機能や病態形成の研究に大きく役立つことが期待できる。 | |
| 2023 | 第46回日本神経科学大会 | 2D and 3D tri-culture system composed of hiPSC derived neurons, astrocytes, and microglia (H. Kobayashi, H. Kato, S. Endoh Yamagami) |
神経変性疾患に深く関与する神経炎症において、ミクログリアの役割が注目されている。iPS細胞由来ミクログリア単独培養では、活性化状態に特徴的なアメボイド型を示したのに対し、アストロサイトや神経細胞と共培養することにより、ミクログリアが健常者のヒト脳内に近い多分岐型の形態を示した。また、炎症刺激であるLPSにより、3者共培養中のミクログリアが多分岐型からアメボイド型へと変化すること、さらには、LPS刺激による細胞の活性化が、ミクログリアからアストロサイトへ伝えられていくことを示した。神経炎症の理解に貢献することが期待できる。 | |
| 2019 | Society of Neuroscience | Induction and characterization of human A1 astrocytes (H. Kobayashi, A. Nabetani, H. Suzuki-Masuyama, W. Shin, K. Maeda, K. Kazetani, T. Wakui, J. Hosokawa, S. Endoh-Yamagami) | 脳内で神経細胞を取り巻くアストロサイトの神経変性疾患への関与が注目されている。アストロサイトが神経傷害型A1に変化し、神経細胞を殺傷することで病気が進むと考えられており、アストロサイトは神経変性疾患の新たな治療標的として期待されている。ヒトiPS細胞由来アストロサイトをA1に変化させる条件を検討し、げっ歯類での報告とは異なる条件を見出した。さらに、遺伝子発現、及び神経傷害性を384スケールにてハイスループットに評価できる系を構築し、A1誘導を抑制する化合物を取得した。アストロサイトを標的とした新規薬剤開発に役立つことが期待できる。 |
論文
| 年度 | 概要 |
|---|---|
| 2025 | Tau aggregation induces cell death in iPSC-derived neurons (Aging Brain Volume 7,2025, 100136)Hirokazu Tanabe, Sumihiro Maeda, Etsuko Sano, Norio Sakai, Setsu EndohYamagami, Hideyuki Okano |
| 2025 | MAPT-A152T mutation drives neuronal hyperactivity through Fyn-NMDAR signaling in human iPSC-Derived neurons: Insights into Alzheimer's pathogenes (Regenerative Therapy Volume 28,March 2025, Pages 201-213), Maika Itsuno, Hirokazu Tanabe, Etsuko Sano, Takashi Sasaki, Chisato Oyama, Hiroko Bannai, Koichi Saito,Kazuhiko Nakata, Setsu Endoh-Yamagami, Hideyuki Okano, Sumihiro Maeda |
| 2019 | Gene grouping strategy for network modeling from a small time-series dataset: An illustrative analysis of human organogenesis – ScienceDirect (Kiyohiro Maeda) Biosystems. 2019 May:179:24-29. |
お見積り・ご注文について
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。