富士フイルム F-hiSIEC™
特長
-
ヒト生体由来腸管上皮細胞と同等のCYP3A4酵素活性
腸管上皮細胞が薬物を吸収する際に、薬物代謝酵素の中で最も重要な機能を果たすCYP3A4の酵素活性がヒト生体由来腸管上皮細胞と同等です。
-
ヒト生体同等の主要トランスポーター遺伝子発現量
薬物の腸管上皮細胞内への取り込みと細胞外への排出をつかさどるトランスポーター遺伝子の発現量がヒト生体由来腸管上皮細胞とほぼ同等です。
-
さまざまな細胞培養容器で使用可能な高い汎用性
プレートやセルカルチャーインサートなどさまざまな細胞培養容器で使用可能です。また、セルカルチャーインサートに播種することで、バリア機能が確保できます。
-
評価アッセイに応じた培養培地の選択
気液培養を行う新培地 Culture Medium AL により、従来の培地よりもヒトとの相関性が高い薬物代謝能予測を行うことが可能です。
培地毎の評価実績
培地毎の評価実績 培養法・培養図 評価例 F-hiSIEC™ Culture Medium 
炎症性試験、バリア機能評価、
腸内細菌との共培養、
ノロウィルスとの共培養、免疫試験F-hiSIEC™ Culture Medium AL 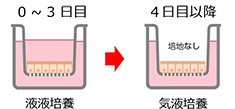
Fg 値予測
F-hiSIEC™ Culture Medium 液液培養による評価例
F-hiSIEC™ Culture Medium による液液培養を行った F-hiSIEC™ の評価データです。
CYP3A4活性
腸管上皮細胞が薬物を吸収する際に、薬物代謝酵素の中で最も重要な機能を果たすCYP3A4の酵素活性が、Caco-2細胞に対して約30倍、ヒト生体由来腸管上皮細胞と同等です。
代謝酵素の遺伝子発現
第1相の薬物代謝酵素(CYP3A4、CYP2C9、CYP2C19、CES2)、第2相の薬物代謝酵素(UGT1A1、UGT2B7、SULT1B1)、二糖加水分解酵素(Sucrase-Isomaltase,Lactase,Trehalase,Maltase-Glucoamylase)について、生体小腸同等の遺伝子発現を⽰しています。






トランスポーターの遺伝子発現
薬物トランスポーター(MDR1、MRP1、MRP2、 MRP3、BCRP、OCT1、OATP2B1)、グルコーストランス ポーター(GLUT2、GLUT5、SGLT1)、ペプチドトランスポーター(PEPT1)、核酸トランスポーター(CNT1、 CNT2、ENT1、ENT2)、コレステロールトランスポーター(ABCG5、ABCG8、NPC1L1)、カルシウムトラン スポーター(CaT1)について、生体小腸同等の遺伝子発現を⽰しています。










腸管上皮細胞マーカー
腸管上皮細胞マーカーについて、⽣体⼩腸同等の遺伝⼦発現を⽰しています。


各種腸管上皮細胞の存在
吸収上皮細胞(VIL1)、 杯細胞(MUC2)、 内分泌細胞(REG4)、 パネート細胞(LYZ)、 M細胞(GP2)、 タフト細胞(DCLK1)のマーカー遺伝子が発現しており、存在が示唆されております。



バリア機能
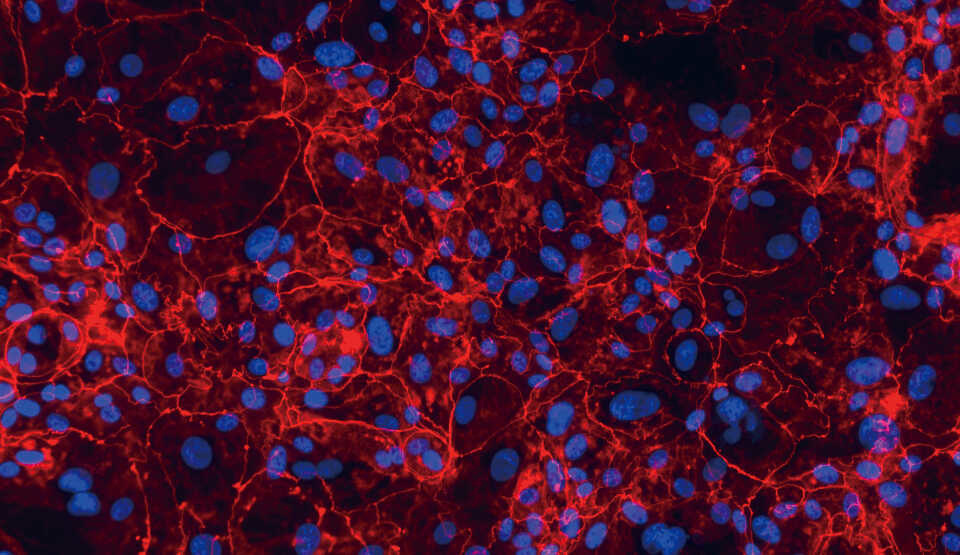 ※ Occludinを免疫染色した画像
※ Occludinを免疫染色した画像
実験条件
- 播種細胞数:10× 104 cells/well
- セルカルチャー インサート:Merck Millipore社製(#MCHT24H48)
- 24 well plate:Greiner Bio-One(#662-160)
安定した性能(ロット間差)
CYP3A4酵素活性及びMDR1(P-gp)トランスポーター活性は、各ロット間で安定した数値を示しています。


本製品はiPSアカデミアジャパン株式会社よりiPS細胞技術に関する特許の非独占的実施権の許諾を受けております。
F-hiSIEC™ Culture Medium による液液培養法スケジュール
本製品は細胞を解凍・播種した翌日から、使用例1の通り、一日おきに培地交換を行ってください。培養9日目~13日目の間で試験実施可能ですが、12日目以降の試験には F-hiSIEC™ Culture Mediumの追加購入が必要です。
土曜日及び日曜日の培地交換を避ける場合は、使用例2の通り、木曜日に解凍・播種し、培養を開始してください。この場合、11日目月曜日から13日目水曜日まで試験実施可能です。
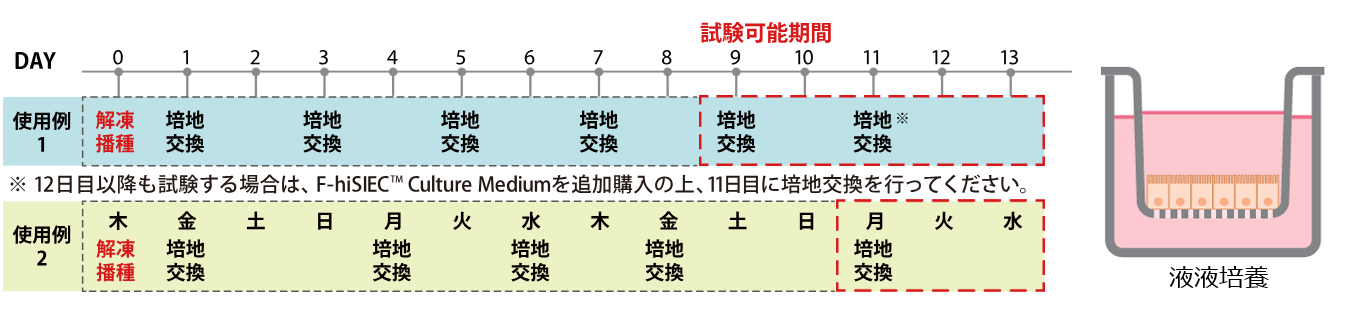 * 初日の播種の際はF-hiSIEC™ Seeding Mediumをご使用ください。
* 初日の播種の際はF-hiSIEC™ Seeding Mediumをご使用ください。* 培養期間中の培地交換の際はF-hiSIEC™ Culture Mediumをご使用ください。
※器材、特にCell Culture Insert はCorning 社製品を推奨します。
- T-issue Culture Plate
- Cell Culture Insert:24 well plate
- ① Corning製トランズウェル(プレートとインサートのセット:#3413)
- ② Greiner Bio-One製(プレート:#662-160、インサート:#662-640)
※試薬は下記を推奨しております。
- Matrigel Matrix Growth Factor Reduced(CORNING #354230)
- DMEM / F12(1:1)(Gibco #11330-032)
- F-hiSIEC™ Seeding Medium
Culture Medium AL と従来 Culture Medium との比較評価データ
F-hiSIEC™ Culture Medium AL は F-hiSIEC™ の気液培養に適した培養培地です。本培養培地をご使用頂くことで、従来の培地よりもヒトとの相関性が高い薬物代謝能予測を行うことができます。
従来の培地 (Culture Medium) との比較評価
遺伝子発現
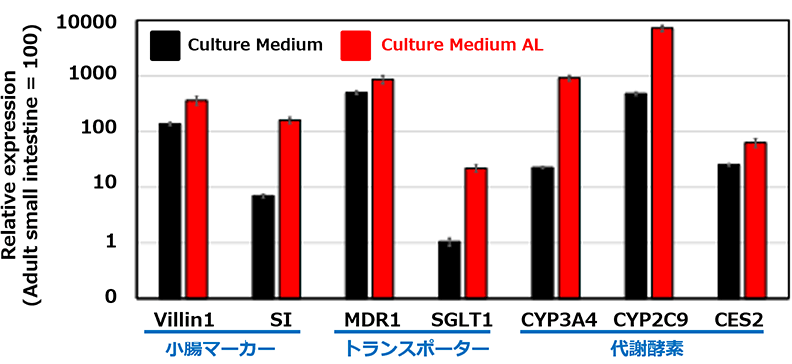
Culture Medium AL で F-hiSIEC™ を培養することにより、従来の培養法よりも小腸マーカー、トランスポーター、代謝酵素などの遺伝子発現が上昇します。
バリア機能
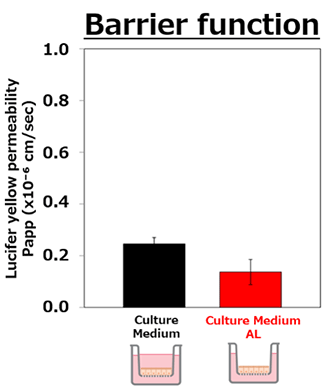
Culture Medium AL による気液培養においても、F-hiSIEC™ のバリア機能が維持されることを確認しました。
播種密度と Fg 値
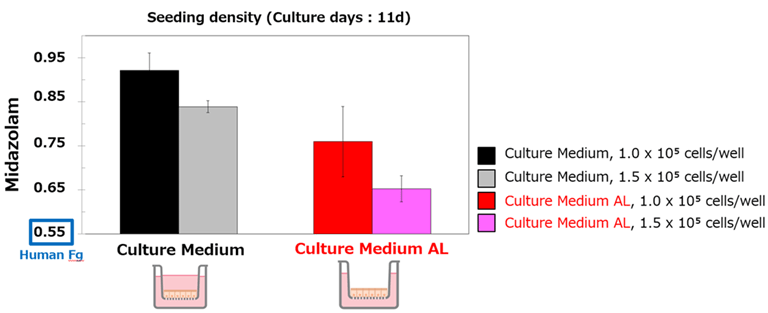
培養 11 日の F-hiSIEC™ におけるミダゾラムの Fg 値は、Culture Medium AL で培養し、播種密度 1.5 x 105 cells/well の条件において、最もヒトの Fg 値 (0.55) に近くなりました。
CYP3A4 基質の Fg 予測
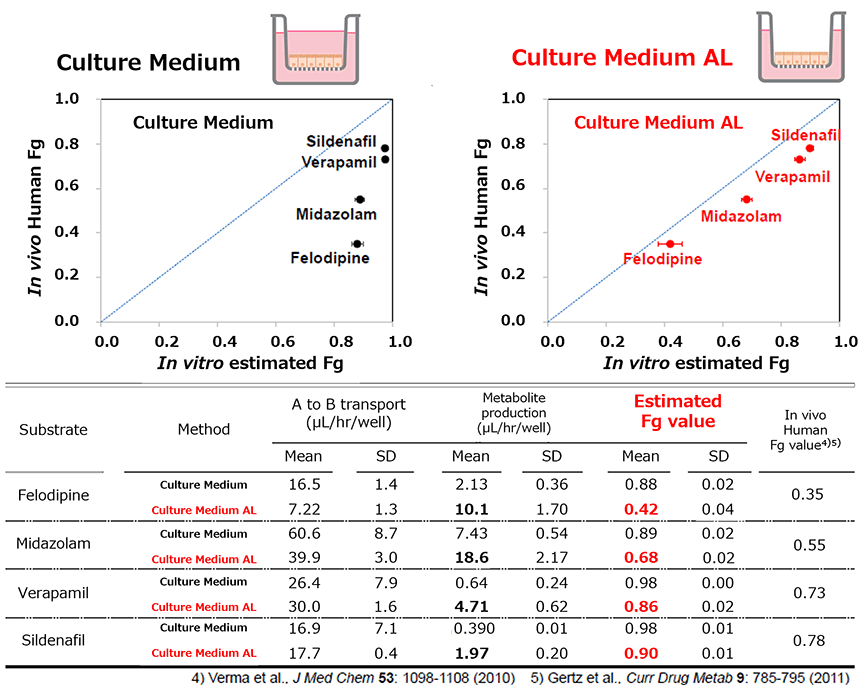
Culture Medium AL で気液培養した F-hiSIEC™ の各種薬剤に対する Fg 値は、ヒト生体における Fg 値と良好な相関関係を示しました。
F-hiSIEC™ Culture Medium AL による気液培養法スケジュール
土曜日および日曜日の培地交換を避けるために、木曜日に解凍、播種し、培養を開始してください。本使用例においては、11 日目月曜日の試験実施を推奨します。また、気液培養は培養 4 日目から開始することを推奨します。
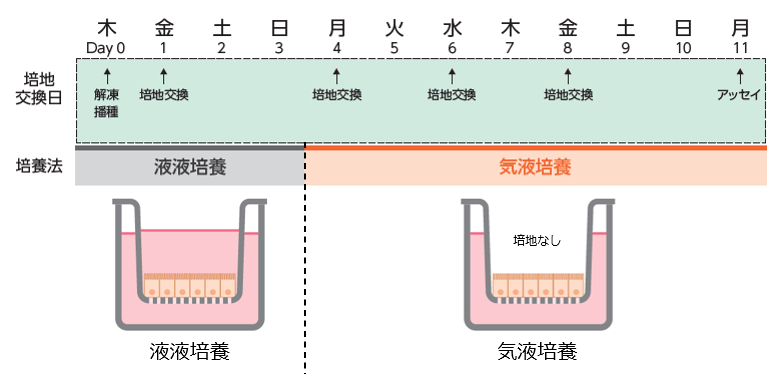
* 初日の播種の際は F-hiSIEC™ Seeding Mediumをご使用ください。
* 培養期間中の培地交換の際はF-hiSIEC™ Culture Medium ALをご使用ください。
※器材、特にCell Culture Insert はCorning 社製品を推奨します。
器材
- Cell Culture Insert : 24 well Plate
Corning 社製トランズウェル(プレートとインサートのセット: #3413)
試薬
- Matrigel Matrix Growth Factor Reduced(CORNING #354230)
- DMEM / F12(1:1)(Gibco #11330-032)
- F-hiSIEC™ Seeding Medium
- F-hiSIEC™
各種資料
取扱説明書

取扱説明書

取扱説明書
SDS
- F-hiSIEC™ 凍結細胞
- F-hiSIEC™ Seeding Medium 播種培地
- F-hiSIEC™ Culture Medium 培養培地
- F-hiSIEC™ Assay Medium CYP3A4 活性測定培地
- F-hiSIEC™ Culture Medium AL
学会発表資料
2025 年 5 月までに公開された F-hiSIEC™ を用いた論文のリストとなります。F-hiSIEC™ を用いて腸管薬物動態、吸収性評価、他細胞および細菌との共培養、そしてウィルス感染性評価等の論文報告がございます。論文へのアクセスには購入が必要な場合がございます。
| 分類 | 時期 | 学会名 | 要旨 | 資料 |
|---|---|---|---|---|
| 免疫・炎症 | 2019年11月 | 日本食品免疫学会 設立15周年記念学術大会 発表ポスター | F-hiSIECの特性、腸管免疫評価への応用 | [PDF] |
| 薬物動態 | 2019年11月 | 日本動物実験代替法学会 第32回大会 発表ポスター | F-hSIECの特性、腸管吸収評価モデルとしての有用性 | [PDF] |
| 薬物動態 | 2019年12月 | 日本薬物動態学会 第34回年会 発表ポスター | F-hSIECの特性、腸管吸収評価モデルの機能 | [PDF] |
| 薬物動態、免疫・炎症、ウイルス | 2020年10月 | iPS細胞由来分化細胞セミナー 発表資料 | 薬物間相互作用評価、腸管免疫評価、腸管ウイルス培養系の可能性 | [PDF] |
| 薬物動態、免疫・炎症、ウイルス | 2020年11月 | 日本動物実験代替法学会 第33回大会 発表ポスター | 薬物動態評価、腸管免疫評価、ウイルス評価への応用 | [PDF] |
| 薬物動態 | 2020年12月 | 日本薬物動態学会年会 第35回年会 発表資料 | 薬物間相互作用評価、動態予測精度改善検討 | [PDF] |
| 免疫・炎症 | 2021年3月 | 日本農芸化学会2021年度大会 | M細胞による取込み機能、Toll様受容体や脂肪酸受容体を介した免疫応答機構 | [PDF] |
| 腸内細菌、免疫・炎症 | 2021年3月 | 第94回日本細菌学会総会 | 腸内細菌機能評価への応用:M細胞による取込み機能、Toll様受容体や脂肪酸受容体を介した免疫応答機構 | [PDF] |
| 免疫・炎症 | 2021年7月 | 第58回日本消化器免疫学会総会 | 消化管炎症モデル、炎症モデルにおける腸内細菌代謝物の影響評価 | [PDF] |
| 毒性評価 | 2021年7月 | 第48回日本毒性学会学術年会 | 消化管毒性評価モデルへの応用:抗がん剤の細胞毒性評価、Notch阻害による分化異常評価 | [PDF] |
| 薬物動態、免疫・炎症 | 2021年11月 | 日本薬物動態学会 第36回年会 | 消化管炎症モデル、M細胞による取り込み評価、薬物動態に関するF-hiSIECを用いた研究例の紹介 | [PDF] |
| 毒性評価、免疫・炎症 | 2022年5月 | 第49回日本毒性学会学術年会 | M細胞によるナノ粒子取込み機能評価、消化管炎症モデルへの応用 | [PDF] |
| 薬物動態 | 2022年11月 | 日本薬物動態学会 第37回年会 発表ポスター | 動態予測精度改善検討、腸管吸収予測性向上の検討 | [PDF] |
| 腸内静菌、免疫・炎症 | 2023年6月 | 第27回腸内細菌学会学術集会 | 嫌気性腸内細菌とF-hiSIECの共培養による相互機能評価 | [PDF] |
| 薬物動態 | 2023年11月 | 日本動物実験代替法学会 第36回大会 | F-hiSIEC改良法(改良培地×改良培養法)による消化管代謝評価 | [PDF] |
| 免疫・炎症 | 2023年11月 | 日本食品免疫学会第19回学術大会 | F-hiSIECの食品免疫研究での応用例:腸管吸収、免疫応答・炎症、腸内細菌共培養 | [PDF] |
| 薬物動態 | 2023年12月 | 第97回日本薬理学会年会 | F-hiSIEC改良法(改良培地×改良培養法)による消化管代謝評価、免疫・炎症評価 | [PDF] |
| 毒性評価 免疫・炎症 | 2024年2月 | ヒト iPS 細胞由来分化細胞の創薬応用 webinar 2024 | ヒトiPS細胞由来腸管上皮細胞(F-hiSIEC)の基本性能および消化管吸収モデル等への活用について | [PDF] |
| 薬物動態 | 2024年6月 | 第31回HAB研究機構学術年会 | 新規培養法によるヒトiPS 細胞由来腸管上皮細胞を用いた薬物のヒト小腸代謝回避率の評価 | [PDF] |
| 毒性評価、 薬物動態 | 2024年7月 | 第51回日本毒性学会学術年会 | ヒトiPS細胞由来腸管上皮細胞(F-hiSIEC)の新規培養法による、薬物代謝能の改善と毒性評価への展開可能性 | [PDF] |
| 代謝機能 | 2024年11月 | 日本動物実験代替法学会 第37回大会 | ヒト iPS 細胞由来腸管上皮細胞における輸送担体及び代謝機能のCaco-2細胞との比較 (膜透過性評価試験受託サービスはこちら) |
[PDF] |
| 毒性評価、薬物動態 | 2024年12月 | 日本食品免疫学会設立20周年記念学術大会 | ヒトiPS細胞由来腸管上皮細胞を用いたヒト腸管モデルの改良と食品免疫研究への応用 | [PDF] |
| 薬物動態 | 2025年5月 | 第32回HAB研究機構学術年会 NEW | Culture Medium AL で培養したヒトiPS 細胞由来腸管上皮細胞 F-hiSIEC の薬物動態評価モデルとしての有用性検討 | [PDF] |
関連論文
細胞特性・アプリケーション全般
- Imakura, Y. et al.: Biochem Biophys Res Commun. 2024 Jan 15:692:149356. Utility of human induced pluripotent stem cell-derived small intestinal epithelial cells for pharmacokinetic, toxicological, and immunological studies
吸収・代謝評価
- Shirai, K. et al.: Drug Metab Pharmacokinet. Available online 31 December 2023, 100994 Air–liquid interface culture and modified culture medium promote the differentiation of human induced pluripotent stem cells into intestinal epithelial cells
- Kitaguchi, T. et al.: ALTEX. 2023;40(4):595-605. In Vitro-Based Prediction of Human Plasma Concentrations of Food-Related Compounds
- Itagaki, M. et al.: J Pharm Sci. 2023 Sep;112(9):2591-2595. Evaluation of Function and Features of Human Induced Pluripotent Stem Cell-Derived Small Intestinal Epithelial Cells for Analyzing Peptide Drug Intestinal Absorption Profiles
- Kitaguchi, T. et al.: Drug Metab Dispos. 2022 Jan;50(1):17-23. Simultaneous Evaluation of Membrane Permeability and UDP-Glucuronosyltransferase–Mediated Metabolism of Food-Derived Compounds Using Human Induced Pluripotent Stem Cell–Derived Small Intestinal Epithelial Cells
- Agustina, R. et al.: Drug Metab Dispos. 2021 Nov;49(11):972-984. Identification of Food-Derived Isoflavone Sulfates as Inhibition Markers for Intestinal Breast Cancer Resistance Proteins
- Kabeya, T. et al.: Drug Metab Pharmacokinet. 2020 Aug;35(4):374-382. Pharmacokinetic functions of human induced pluripotent stem cell-derived small intestinal epithelial cells
腸内細菌共培養・ウイルス培養※In vitro ヒトノロウイルス(HuNoV)消毒効果 評価サービスはこちら
- Sen, A. et al.: Front Microbiol. 2023 Apr 13:14:1155438 Comprehensive analysis of metabolites produced by co-cultivation of Bifidobacterium breve MCC1274 with human iPS-derived intestinal epithelial cells
- Yamada, S. et al.: J Pharmacol Sci. 2022 Jul;149(3):139-146. SARS-CoV-2 induces barrier damage and inflammatory responses in the human iPSC-derived intestinal epithelium
- Soh Yamamoto. et al.: , Scientific Reports., Jul; 14, 15181 (2024)
MPS(生体模倣システム)
- Shinha, K. et al.: Micromachines (Basel). 2021 Aug 24;12(9):1007. A Kinetic Pump Integrated Microfluidic Plate (KIM-Plate) with High Usability for Cell Culture-Based Multiorgan Microphysiological Systems
製品一覧
- 項目をすべて開く
- 項目をすべて閉じる
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。