【テクニカルレポート】PSアフィニティー法が実現した高活性なMSC由来エクソソームの精製 −エクソソーム再生医療における全く新たな戦略の提案−
本記事は、和光純薬時報 Vol.88 No.4(2020年10月号)において、富士フイルム和光純薬 導入品推進部 学術課 山根 昌之、ライフサイエンス研究所 石止 貴将が執筆したものです。
細胞外小胞のひとつであるエクソソームは、細胞が放出する脂質二重膜の小胞体である。近年、間葉系幹細胞(Mesenchymal stem cell : MSC)など一部の細胞に由来するエクソソームに治療効果が存在することが示されたことから、エクソソームを利用した再生医療が注目されている。本稿では当社が開発したエクソソーム精製技術である PS アフィニティー法の利点と最近明らかになった再生医療における有用性について紹介する。
エクソソーム
エクソソームは細胞から放出されるCD9、CD63、及び CD81 などをマーカータンパク質とした直径 30 ~ 100nm の脂質二重膜の小胞体である 1)。エクソソームはタンパク質や DNA、RNA、さらには脂質といった細胞由来成分を含んでおり、これらの受け渡しによる細胞間情報伝達に関与すると考えられている 2)。
MSC由来エクソソーム
MSC は、脂肪、骨、及び軟骨への分化が可能な中胚葉由来の幹細胞である。MSC は骨髄や脂肪、臍帯から樹立できることから再生医療のソースとして期待されている。この MSC は免疫抑制や抗炎症、抗線維化といった効果を有することが知られているが、近年これらがエクソソームによるものであることが示されている 3)。このことから、MSC 由来エクソソームを利用する再生医療が注目されはじめている。
新規エクソソーム精製手法(PSアフィニティー法)
エクソソームの精製には、古くから用いられてきた超遠心分離法をはじめ、密度勾配分離法や表面抗原を利用した抗体アフィニティー法などが知られているが 4)、いずれも回収率、精製純度、インタクトな粒子の取得、再現性においてそれぞれ課題を有している。
これに対し当社は、エクソソームの表面に存在するホスファチジルセリン (Phosphatidylserine : PS) を利用した新たな精製手法である PS アフィニティー法を金沢大学の華山教授らと共同開発した 5)。PS アフィニティー法ではカルシウム依存的に PS に結合する Tim4 タンパク質が使用される。この Tim4 タンパク質は PS に対して強力に結合する一方、EDTA のようなカルシウムキレート剤の作用によりその結合が乖離する。このような性質を利用して、回収率、精製純度、インタクトな粒子の取得、再現性において従来法より有効なエクソソーム精製が可能になった (図 1)。
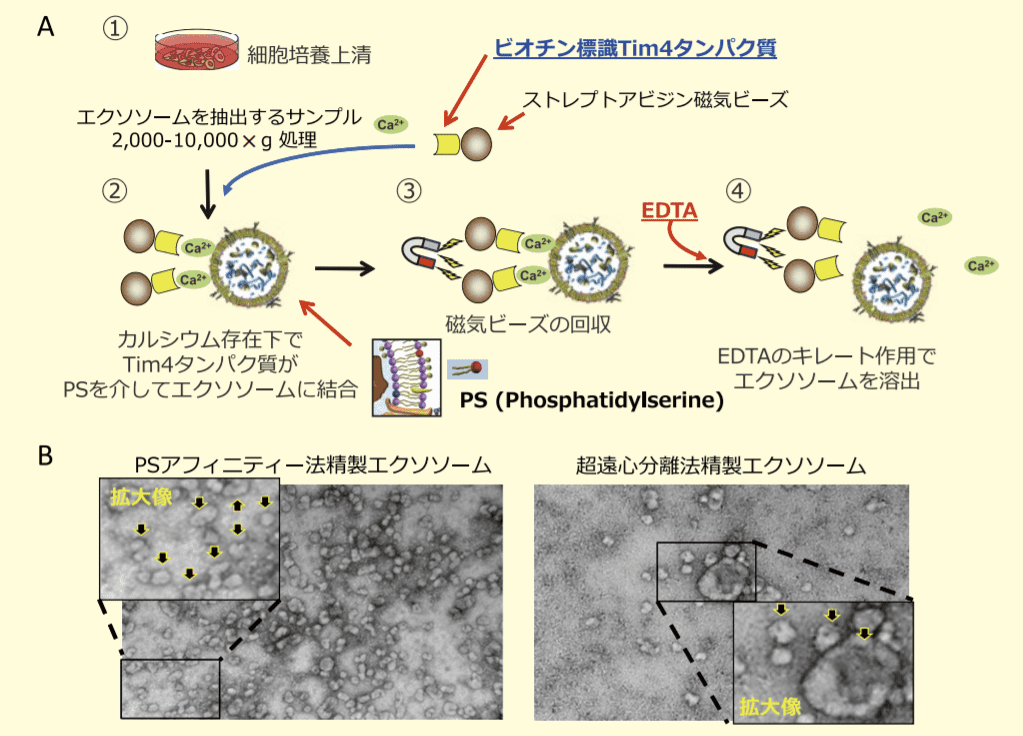
図1.
A)PS アフィニティー法によるエクソソーム精製のフロー。B)PS アフィニティー法、及び超遠心分離法により精製した COLO201 細胞株由来エクソソームを透過型電子顕微鏡により撮影した像。矢印はエクソソームを示す。PSアフィニティー法が実現した高活性なMSC由来エクソソームの精製
今回当社が新たに明らかにしたMSC 由来エクソソームの精製における PS アフィニティー法の有用性について以下に紹介する。はじめに、骨髄由来 MSC の培養上清から PS アフィニティー法及び超遠心分離法で精製を行い、PS アフィニティー法を応用したエクソソーム定量技術である PS ELISA 法 (図 2A) によりエクソソーム回収率の比較を行った。CD9、CD63 及び CD81 の検出からエクソソームの定量解析を行ったところ、超遠心分離法では 40% 程度の回収率であるのに対し、PS アフィニティー法では 80% 以上と極めて高い回収率を示すことが確認された (図 2B)。
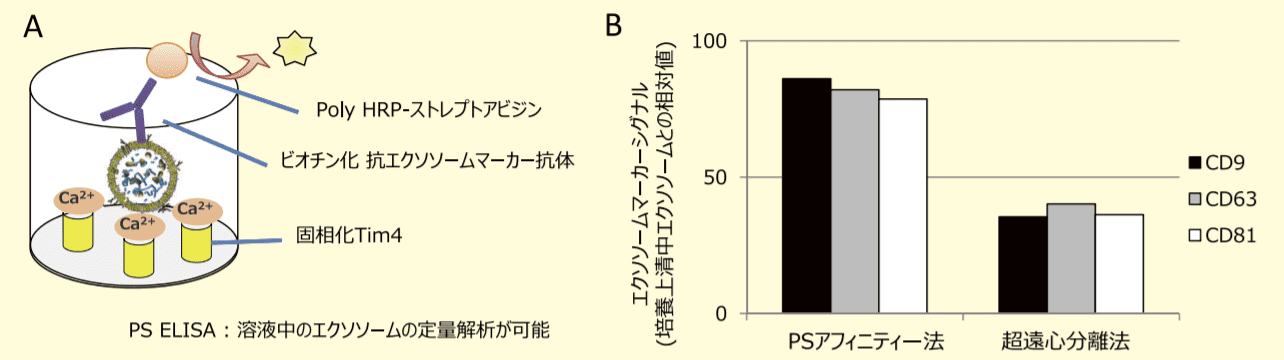
図2.
A)PS ELISA 法の原理。固相化した Tim4 タンパク質で捕捉したエクソソームを表面抗原を認識する抗体で検出することで定量解析を行う当社独自の技術。B)PS ELISA法により PS アフィニティー法、超遠心分離法それぞれの手法で精製した MSC 由来エクソソームを定量した結果。検出には抗 CD9 抗体、抗 CD63 抗体、抗 CD81 抗体を使用。グラフは培地中のエクソソームとの相対値。PS ELISA 法:PS Capture™ Exosome ELISA Kit(Streptavidin HRP)(コード No. 298-80601; 抗 CD63 抗体付属); 抗 CD9 抗体(コード No. 019-27953)、抗 CD81 抗体(コード No. 011-28111)さらに、両手法で精製した MSC 由来エクソソームの活性を比較するため、ヒト末梢血由来単核球 (PBMC)由来単球を用いた抗炎症効果及びヒト胎児肺由来正常線維芽細胞 (TIG3 細胞) を用いた抗線維化効果の検討を実施した。その結果、PS アフィニティー法で精製した MSC 由来エクソソームが超遠心分離精製エクソソームに比べ、極めて高い活性を有していることが明らかとなった (図 3,図 4)。
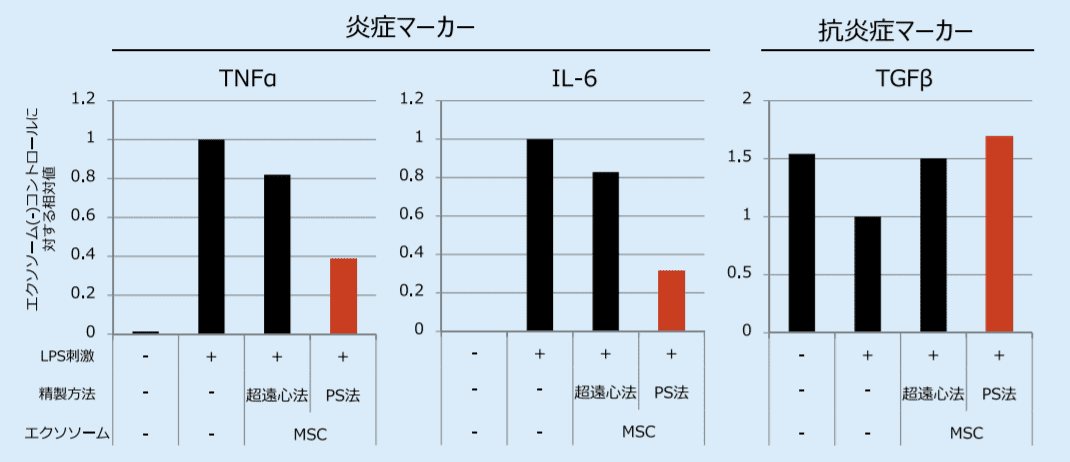
図3.PBMC 由来単球を LPS で刺激して誘導した炎症に対する MSC 由来エクソソームの効果を定量 PCR により検討した結果
各手法で精製した MSC 由来エクソソームを 4.5×108 particles/mL で添加している。TNFα、IL-6 の上昇、及び TGFβの低下は MSC 由来エクソソームにより抑制されることを確認した。さらにこのような効果は超遠心分離法に比べ PS アフィニティー法で精製したエクソソームがより強力であることも確認した。超遠心法:超遠心分離法、PS 法:PS アフィニティー法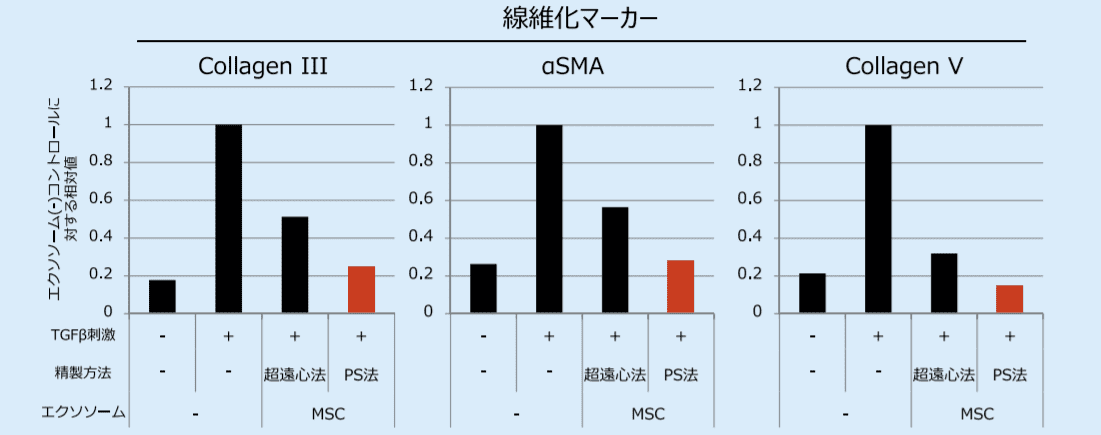
図4.TIG3 細胞を TGFβで刺激して誘導した線維化関連遺伝子の上昇に対する MSC 由来エクソソームの効果を定量 PCR により検討した結果
各手法で精製した MSC 由来エクソソームを 1×109 particles/mL で添加している。Collagen III、αSMA、Collagen V の上昇は MSC 由来エクソソームにより抑制されることを確認した。さらにこのような効果は超遠心分離法に比べ PS アフィニティー法で精製したエクソソームがより強力であることも確認した。超遠心法:超遠心分離法、PS 法:PS アフィニティー法以上の結果は、PS アフィニティー法が MSC 由来エクソソームを高回収率かつ高活性を保持した状態で精製することが可能であることを意味する。逆に言えば、従来法の課題である低い回収率に加え、超遠心の物理的ダメージによる MSC 由来エクソソームの活性低下が今回改めて浮き彫りになったものと考えられる。よって、当社が開発した PS アフィニティー法は、今後のエクソソーム治療分野において、革新的な技術に成り得るポテンシャルを十分に秘めていると言える。
最後に
繰り返しになるが、エクソソームを用いた再生医療が注目される一方で、現状では超遠心分離法といった古典的な精製手法が依然として広く利用されている 6)。これに対して当社が開発した PS アフィニティー法は、エクソソームの回収率、精製純度、インタクトな粒子の取得、再現性に優れた精製手法であり、従来法の問題点である低い回収率と活性低下を解決した理想的な手法である。今後再生医療に最適化したエクソソーム精製技術が必要になることが予想されるが、PS アフィニティー法が極めて強力な技術ツールになることを期待している。
参考文献
- Colombo, M. et al . : Annu. Rev. Cell Dev. Biol., 30, 255 (2014). DOI: 10.1146/annurev-cellbio-101512-122326
- Mathieu, M. et al. : Nat. Cell Biol., 21 (1), 9 (2019). DOI: 10.1038/s41556-018-0250-9
- Phinney, D. G. and Pittenger, M. F. : Stem Cells, 35 (4), 851 (2017). DOI: 10.1002/stem.2575
- Thery, C. et al. : Curr. Protoc. Cell Biol., 30 (1), 3. 22. 1 (2006). DOI: 10.1002/0471143030.cb0322s30
- Nakai, W. et al. : Sci. Rep., 6, 33935 (2016). DOI: 10.1038/srep33935
- Fujita, Y. et al. : J. Clin. Med., 7 (10), 355 (2018). DOI: 10.3390/jcm7100355















